Nel 1935, Stein e Leventhal, definirono per la prima volta la PCOS come un quadro clinico caratterizzato da: oligomenorrea, irsutismo, obesità e spesso, Acanthosis nigricans (manifestazione cutanea caratterizzata da zone iperpigmentate, mal delimitate, che compaiono tipicamente a livello delle pieghe cutanee (collo, ombelico, inguine, ascelle). La pelle si presenta ispessita e vellutata, di colore più scuro (dal brunastro al nero) rispetto alle zone circostanti).
La sindrome è estremamente eterogenea, con quadri clinici sfumati o poco caratteristici (es. pazienti affette ma normopeso).
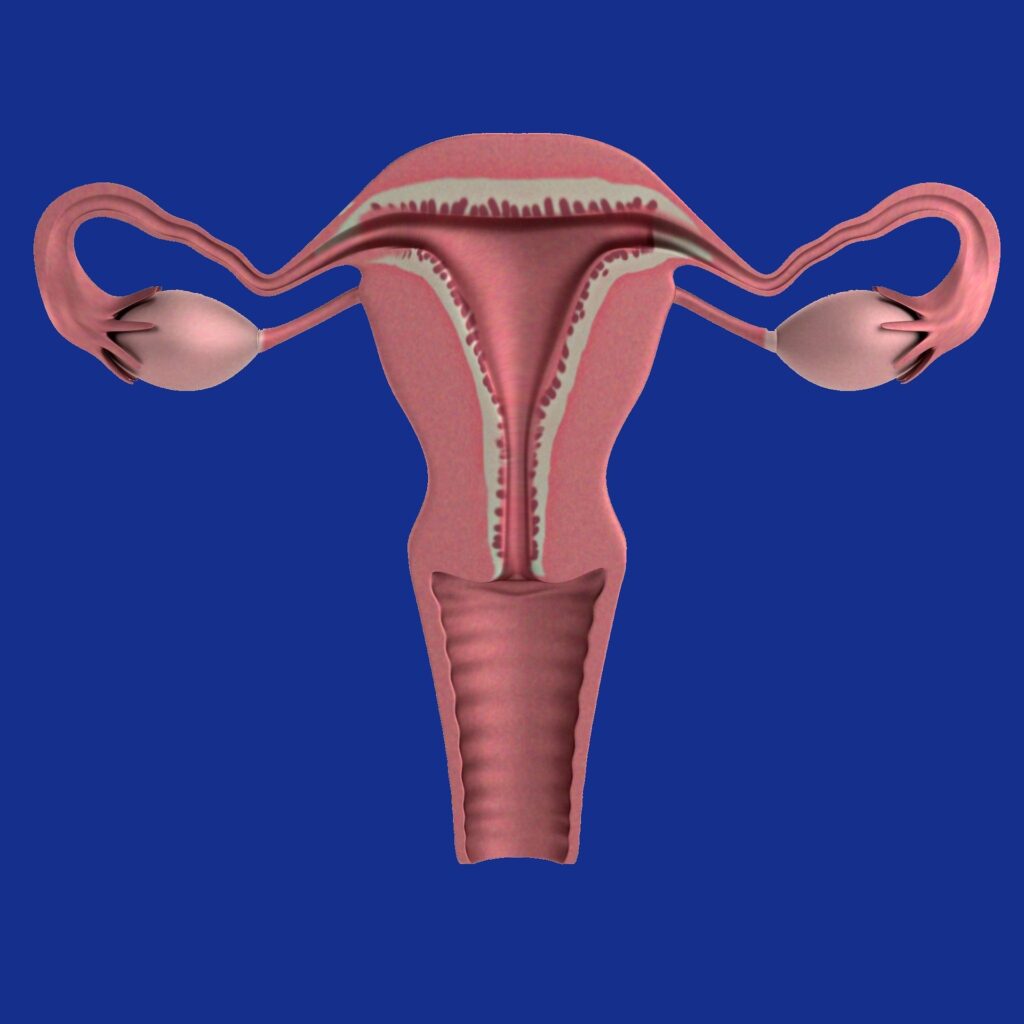
Da un punto di vista ecografico, essa è caratterizzata dalla presenza di ovaie aumentate di volume, con la presenza di numerose e grossolane formazioni cistiche.
La PCOS è associata ad insulino-resistenza ed iperinsulinemia (causa dell’Acanthosis), e nel 1980 venne definitivamente confermata l’alta frequenza di alterazioni metaboliche glucidiche nelle pazienti affette, fino a sfociare in una vera e propria sindrome metabolica (sindrome X).
La PCOS spesso ha un’elevata familiarità, tanto da suggerire un back-ground genetico predisponente, non di tipo mendeliano, ma piuttosto multigenico con fattori ambientali. Il difetto costituzionale che è alla base della sua fisiopatologia consiste in una iperproduzione di androstenedione (ormone steroideo prodotto dal surrene e dalle gonadi) con ridotta risposta in vivo allo stimolo fornito da concentrazioni fisiologiche di FSH (ormone follicolo-stimolante).
La correlazione tra iperandrogenismo ed alterazione del metabolismo dei carboidrati è nota gà dal 1921. In effetti, un’ insulino-resistenza, definibile come l’incapacità di una nota quantità di insulina di aumentare l’uptake e l’utilizzazione del glucosio è frequente nelle pazienti PCOS obese (BMI>25), ma anche nelle normopeso. Ne deriva che l’insulino-resistenza è geneticamente associata alla PCOS, indipendentemente dalla massa grassa e dal BMI e l’obesità determina un aggravamento del quadro clinico verso forme franche di diabete mellito.
Studi di linkage genetico per identificare loci genetici di suscettibilità, hanno consentito di dimostrare che l’Inositolo agisce come mediatore intracellulare dell’insulina. Esso ha 2 principali stereosomeri, il Myo inositolo (MYO) e il D-Chiro-inositolo (DCI). Il MYO o vitamina B7, è un nutriente fondamentale, idrosolubile come le vitamine del gruppo B, non viene immagazzinato nell’organismo, che ne produce tuttavia piccola parte, ma viene assorbito attraverso gli alimenti, in particolare lievito di birra, agrumi, cereali integrali, tuorlo d’uovo, noci, banane. In realtà fa parte delle non vitamine e la sua azione è strettamente legata ad altre vitamine del gruppo B, come biotina, acido folico e pantotenico. Il suo fabbisogno giornaliero è di 500 mg.
Nel plasma, la concentrazione ideale tra MYO e DCI è di 40:1, e nei tessuti il loro rapporto è regolato dall’enzima EPIMERASI. Il MYO migliora la funzionalita’ ovarica, con uptake del glucosio cellulare, sulla qualità e maturità ovocitaria. Nel fegato e nei tessuti responsabili dello stoccaggio del glicogeno, esso favorisce l’uptake del glucosio cellulare. Il DCI non ha nessuna influenza sulla funzione ovarica, ma attraverso la conversione del glucosio in glicogeno (stoccaggio intracellulare), comporta una riduzione dell’iperinsulinemia periferica.
In condizioni patologiche(PCOS ed insulino-resistenza) in cui il rapporto tra i 2 stereoisomeri non è più di 40:1 ,il MYO(MYO——-epimerasi>DCI) a livello ovarico si ha riduzione dell’uptake del glucosio cellulare, riduzione della qualità e maturità ovocitaria; a livello epatico aumento dell’uptake del glucosio cellulare con diminuzione della conversione del glucosio in glicogeno. Pertanto occorre riequilibrare il rapporto fisiologico delle concentrazioni tra MYO e DCI, con la supplementazione farmacologica ed alimentare di MYO e DCI insieme ad acido folico, per consentire la diminuzione delle conseguenze riproduttive metaboliche dell’insulino resistenza e dell’obesità. Infatti il MYO migliora la qualità ovocitaria ed embrionaria rispetto al solo supplemento con DCI e riduce le unità di r-FSH adoperate nei cicli di IVP ed inoltre migliora la sensibilità dei tessuti all’insulina in donne con PCOS insulino-resistenti ed obese. Pertanto, le nuove terapie farmacologiche, che escludono l’uso della metformina, un’ adeguato apporto alimentare ed una corretta attività fisica, consentono nella grande maggioranza dei casi il ripristino della funzionalità ovarica, la riduzione dell’obesità ed il miglioramento del quadro metabolico.
“LE INDICAZIONI CONTENUTE IN QUESTO SITO NON DEVONO IN ALCUN MODO SOSTITUIRE IL RAPPORTO CON IL MEDICO. E’ PERTANTO OPPORTUNO CONSULTARE SEMPRE IL PROPRIO MEDICO CURANTE E/O LO SPECIALISTA”